

2026年4月9日,血液学权威期刊《Haematologica》在线发表两篇关于不典型急性早幼粒细胞白血病(aAPL)的通讯论文。两项研究由陆道培分子医学团队分别携手山西医科大学第二医院与泰安市中心医院完成,分别揭示了两种不同的aAPL发病和对全反式维甲酸(ATRA)原发耐药的新分子机制。
文章一:
助力山西医大第二医院和山西中医药大学王宏伟教授和徐智芳教授团队,报道新融合基因并再次验证“三段式融合”耐药机制

论文题目:Novel ligand-binding domain truncated CPSF7::RARA::CPSF7 tripartite fusion confers primary ATRA resistance in atypical acute promyelocytic leukemia
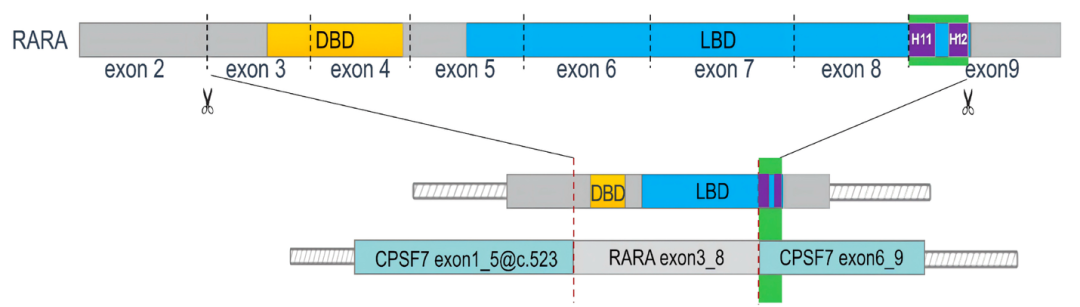
核心发现
首次报道新维甲酸受体(RAR)融合伙伴基因CPSF7,进一步拓展了aAPL中融合基因的多样性。
再次验证此前由陆道培分子医学团队领衔发现的“三段式融合”基因的重现性,及其对原发ATRA耐药的关键作用。
陆道培分子医学团队的刘红星研究员为本论文的共同通讯作者。
文章二:
与泰安市中心医院刘芹芹主任合作,揭示“两段式融合+顺式突变”耐药新机制

论文题目:Bipartite NUP98::RARA-E412* fusion with a cis-aligned ligand binding domain truncation mutation in atypical acute promyelocytic leukemia
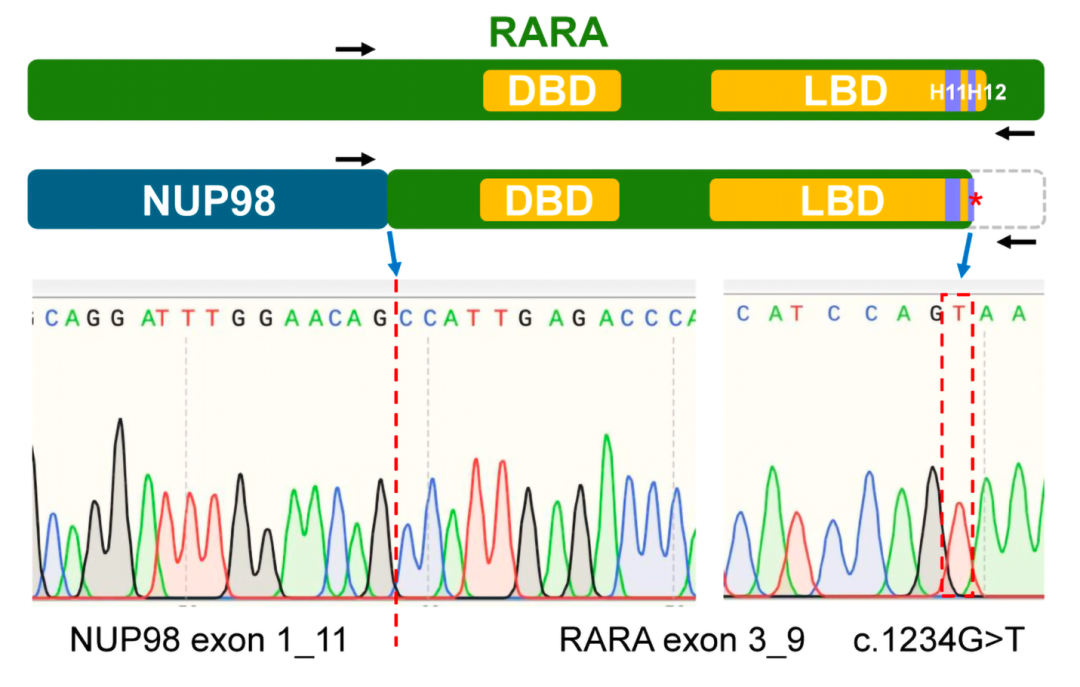
核心发现
报道一种全新发现的发病和耐药机制:即“两段式RAR融合合并顺式截短型突变”导致的APL发病和原发ATRA耐药。
研究首次在NUP98::RARA融合的aAPL病例中发现,患者虽然携带的是两段式融合基因,但在融合转录本中同时携带了配体结合结构域的无义突变。
异曲同工的致病机理:研究中进一步明确,这个顺式突变直接导致LBD结构域中关键的第12个螺旋结构(H12)发生截短。这种由突变介导的LBD截短机制,在功能上与之前发现的“三段式融合”殊途同归,使白血病细胞彻底失去了对ATRA的敏感性,是另一种导致aAPL发病和对ATRA原发耐药的关键分子机制。
陆道培分子医学团队的陈佳琦博士和周晓苏博士为本论文的共同第一作者,刘红星研究员为主要通讯作者。
这两篇同期发表于国际权威期刊的“姊妹篇”研究,进一步丰富了aAPL的分子遗传学图谱,并系统揭示了新的发病机制及原发ATRA耐药分子基础。相关发现不仅对患者的精准诊断与临床决策具有直接指导意义,也为后续新型治疗策略的研究提供了重要方向。
陆道培分子医学团队近年来联合国内多家兄弟医院,持续推动aAPL领域的研究进展,并积极推动从分子认知走向精准诊疗实践,展现出在该领域的引领性影响力。
两篇论文均可于 《Haematologica》 期刊官网免费下载。
作者简介

陈佳琦 博士
河北燕达陆道培医院分子医学室、北京陆道培血液病研究院
吉林大学药理学博士,2017年加入陆道培分子医学团队,主要负责药物基因组项目临床应用及相关研究,复发难治及不典型APL项目组主要成员之一。发表学术论文30余篇,多次于ASH、JSH、KCA、ISLH等国际国内会议进行学术报告和交流。

周晓苏 博士
北京陆道培血液病研究院精准医学中心
副研究员;北京“亦城优秀人才”,中国海洋大学博士、北京协和医学院博士后。博士后出站后加入陆道培分子医学团队,主要从事血液肿瘤分子诊断技术的研发和免疫治疗相关的研究,后转入血液病研究院,负责基因功能和致病机制研究。
中国抗癌协会肿瘤基因诊断专委会委员、北京非公立医疗机构协会检验医学专委会委员等。以第一作者在 Blood, American Journal of Hematology 及 Haematologica 等期刊发表论文数篇,部分成果获期刊封面论文和特邀专家点评。

刘红星 院长
北京陆道培血液病研究院执行院长;陆道培医院病理和检验医学科主任
研究员、检验/病理执业医师。从事临床医师工作 3 年,血液病实验诊断和相关研究工作 23 年。在白血病新分子分型和致病分子机制方面有多项国际原创性新发现或国际领先的研究成果,对血液病的精准诊断和治疗改进有直接的帮助,影响和改写着血液病国际诊疗指南。相关研究成果以通讯/第一作者于 Nature Medicine、Blood、Science Bulletin、Blood Cancer Journal、Amercian Journal of Hematology 等学术期刊发表论文 170 余篇。
